Constante De Disociacion Del Agua
Su producto iónico se mantiene constante de. 28 09 2020 Entregado.
Constante De Disociacion H20 Pdf Disociacion Quimica Equilibrio Quimico
Su constante de equilibrio es.

Constante de disociacion del agua. About Press Copyright Contact us Creators Advertise Developers Terms Privacy Policy Safety How YouTube works Test new features Press Copyright Contact us Creators. QuímicaDesdeCero Química Como ha visto la fuerza de los ácidos varía con el grado de disociación en agua. Dado que la disociación de los ácidos fuertes en.
Constante de disociación del agua. Por lo tanto se incorpora a la constante de disociación k se obtiene una nueva constante que se denomina producto iónico del agua y se representa como kw. H2O H3O OH.
DISOCIACIÓN en química es un proceso general en el cual complejos moléculas yo sales se separan en moléculas más pequeñas iones o radicales usualmente de manera reversible. 3 Modelo Unos cuantos cálculos bastan para demostrar que al mezclar un ácido débil HZ con la sal sódica de dicho ácido NaZ el porcentaje de HZ que se disocia para formar iones H es insignificante en comparación con la cantidad que permanece sin disociar. El valor de K w medido a 24º C es 10-14 moles 2 litro-2Como este valor es constante las concentraciones de H y OH-guardan una relación inversa.
El agua tiene la propiedad de que esta disociación es muy débil. En el agua pura las concentraciones de los. Lo que se cuestiona es qué se mide y la parte conceptual de la medida.
En la cual la proporción de moléculas disociadas es muy baja. El pH como cambio en la estructura del agua. Por esta razón la concentración de H 2O puede considerarse prácticamente constante con lo cual podemos aplicar el principio de un sistema en equilibrio heterogéneo donde el.
El agua H2O tiene la propiedad de que puede disociarse en sus iones. Por tanto la disociación del agua no es constante ni existe como tal. Conociendo la masa molar del agua 18 gramos mol y dejar de lado la concentración de moléculas disociadas y tomando la masa de 1 dm3 de agua por 1000 g se puede calcular la concentración de moléculas no disociadas en 1 dm3 de agua H2O 1000 180153 5551 mol dm3Luego de la ecuación de la constante de disociación del producto se pueden encontrar concentraciones de.
2H 2 O OH- H 3 O Los productos de ésta reacción son los iones oxonio o iones hidronio y los hidroxidos. Debido a que los iones OH y H solo se forman por disociación del agua sus concentraciones deben ser iguales. 05102014 5 Aplicación de la disociación.
El valor de Kw medido a 24 C es 10-14 moles2 litro-2. La constante de disociación del agua expresada por K e K w en inglés es la constante de reacción asociada a la reacción química de autoprotolisis. Perteneciente al agua se rompen debido a una fisión de tipo heterolítica hecho que produce un protón así como también un ión negativo.
En este experimento se determinará la constante de disociación ácida del ácido acético por medio de mediciones de pH. Para entender el proceso de disociación se hace necesario el uso de una constante de equilibrio conocida como constante. Según la ley de acción de masas LAM.
Debido a la alta polaridad de las moléculas de agua entre ellas se forman puentes de hidrógeno y como consecuencia una molécula de agua tiene la capacidad de ceder un protón a la molécula vecina y esto ocasiona que la molécula que cedió su protón quede con una carga neta negativa y la molécula de agua que lo acepta quede con una carga positiva. Como la concentración del agua no disociada es muy grande 555 M y permanece prácticamente inalterada su valor se incluye en la constante que pasa a llamarse producto iónico del agua Kw. K 𝐻 𝑂𝐻 𝐻2 𝑂 18 𝑥1016 𝒌𝒘 𝒌.
Kw H3O OH- 10 10-14. Un mol de agua pesa 18 gramos por lo que en 1 litro de agua 1000 gramos habrá 5555 moles es decir la concentración será 5555 M. En este ensayo se cuestiona la teoría actualmente aceptada para la disociación del agua ya que un protón H no puede existir como partícula aislada conside-rando las características de la estructura del agua Bernal y Fowler 1933.
30 09 2020 Pre-Reporte de Práctica 2. La Constante de Disolución del Agua Kw. Disociación del agua y pH.
No hay discusión sobre la utilidad del pH en los procesos biológicos químicos e industriales. Esto quiere que el agua está formada por una mezcla de H2O y sus iones H3O y OH. A partir de la concentración de protones puede determinarse el pH del agua sabiendo que.
Como la concentracin del agua no disociada es muy grande 555 M y permanece prcticamente inalterada su valor se incluye en la constante que pasa a llamarse producto inico del agua Kw. La constante de autoprotólisis de H 2 O tiene el símbolo especial K W donde W significa water agua en ingles como las concentraciones de lo iones H y OH-a 25 C son 1 u 10-7 M molar mientras que la concentración de agua es 556 M es una constante por lo tanto la constante de disociación del agua queda expresada como. Kw constante de disociación del agua o de autoprotólisis 110-14 o producto iónico del agua.
La disociación del agua representa una situación de equilibrio. Siendo Kc la constante de disociación del agua debido a que la disociación esprácticamente siempre la misma se puede combinar con una nueva constante Kw. Su producto iónico se mantiene constante de manera que podemos establecer una constante de disociación para el agua o que denominaremos KW y cuyo valor a 25ºC viene dado por la siguiente fórmula.
El agua tiene la propiedad de que esta disociación es muy débil. La concentración del agua 5556 molar no se altera con la disociación de los iones por lo que se considera constante. Su constante de disociación es igual al producto de las concentraciones de protones y oxhidrilos dividido por la concentración del agua no disociada.
K w se conoce como constante del producto iónico del agua. Sustancia que al disolverse en agua H2O genera iones H los ácidos se clasifican en fuertes fuerza. 28 09 2020 Revisado.
Kₐ-Constante de disociación ácida Kb-Constante de disociación básica Kw-Constante del producto iónico del agua. Para el caso de las moléculas de agua el concepto de disociación debe revisarse Aceves 1990.
Disociacion Del Agua Pdf Ph Equilibrio Quimico
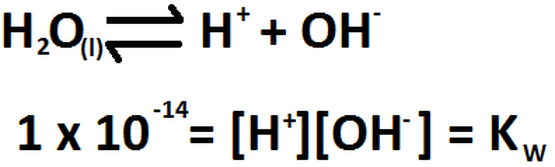
Reacciones En Una Disolucion Acido Base

Concepto De Ph Y Disociacion Del Agua Youtube

La Constante De Disolucion Del Agua Kw Quimica Wikisabio
Disociacion Del Agua Y Ph Unidad De Apoyo Para El Aprendizaje

Constante De Ionizacion Del Agua Qb317 Youtube
Analisis De La Teoria Aceptada Sobre La Disociacion Del Agua

Disociacion Del Agua Y Ph Ph Disociacion Del Agua Udocz

Tema Ionizacion Del Agua Disociacion Del Agua La Escala De Ph Concepto Indicadores De Ph Tema Ionizacion Del Ppt Descargar
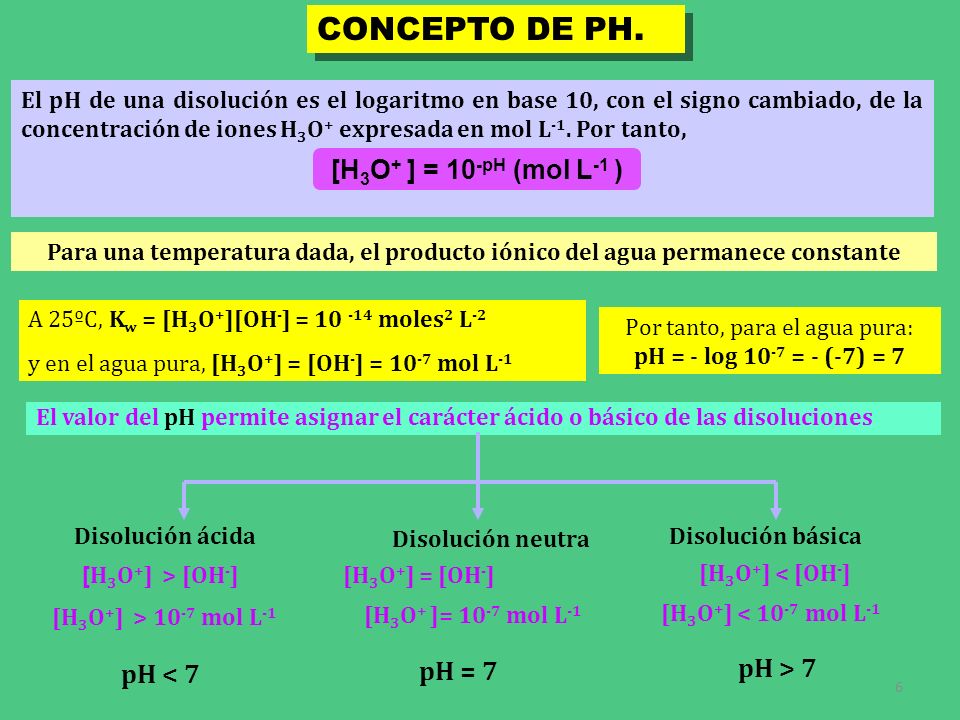
Tema Ionizacion Del Agua Disociacion Del Agua La Escala De Ph Concepto Indicadores De Ph Tema Ionizacion Del Ppt Descargar
3 6 4 Autoionizacion Del Agua Y Escala De Ph Quimica General
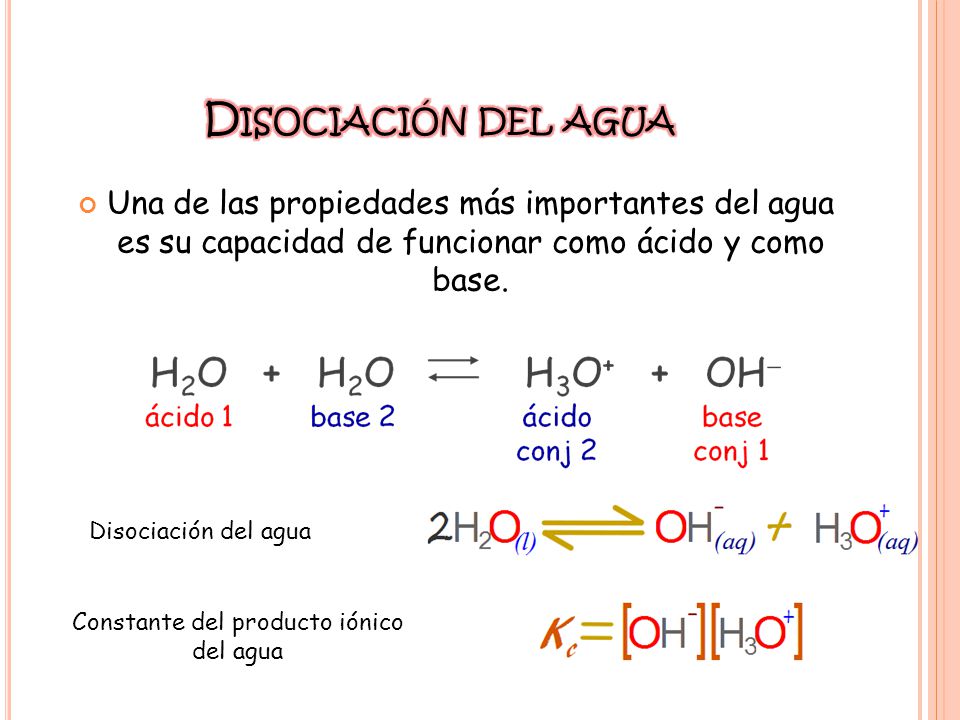
Cinetica Y Equillibrio Quimico Ppt Descargar

Producto Ionico Del Agua Libro Electronico De Bioquimica Juan Jose Martinez Guerra

H2o Estructura Del Agua Ionizacion Del Agua Disociacion Del Agua Ppt Descargar
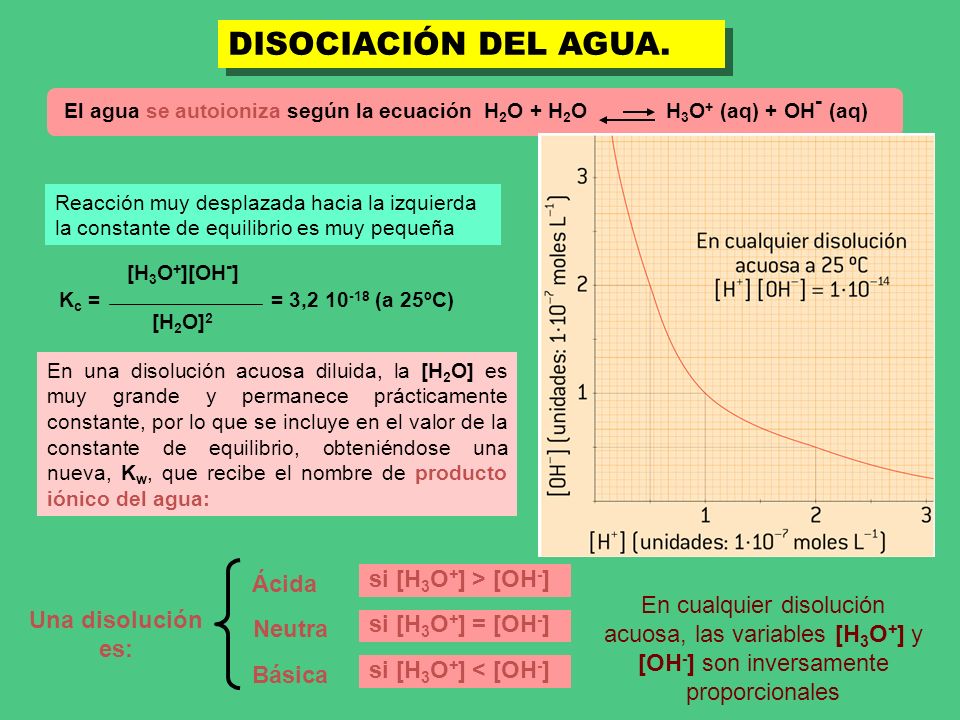
Tema Ionizacion Del Agua Disociacion Del Agua La Escala De Ph Concepto Indicadores De Ph Tema Ionizacion Del Ppt Descargar
Analisis De La Teoria Aceptada Sobre La Disociacion Del Agua








Posting Komentar untuk "Constante De Disociacion Del Agua"